2026年3月6日,我院姬峻芳实验室于Cancer Cell International在线合作发表题为“A New Inject-embed 3D Culture Method Enables the Spheroid and Aggregate Formation from Single or Dual Liver Cancer Cell Types”的研究论文。该研究建立并验证了一种名为“inject-embed”的新型三维细胞培养方法,通过在液体-基质界面同时支持细胞-细胞、细胞-基质的相互作用,促进肝癌细胞在三维微环境中的球体/聚集体形成、组装与功能表型呈现(Fig 1)。
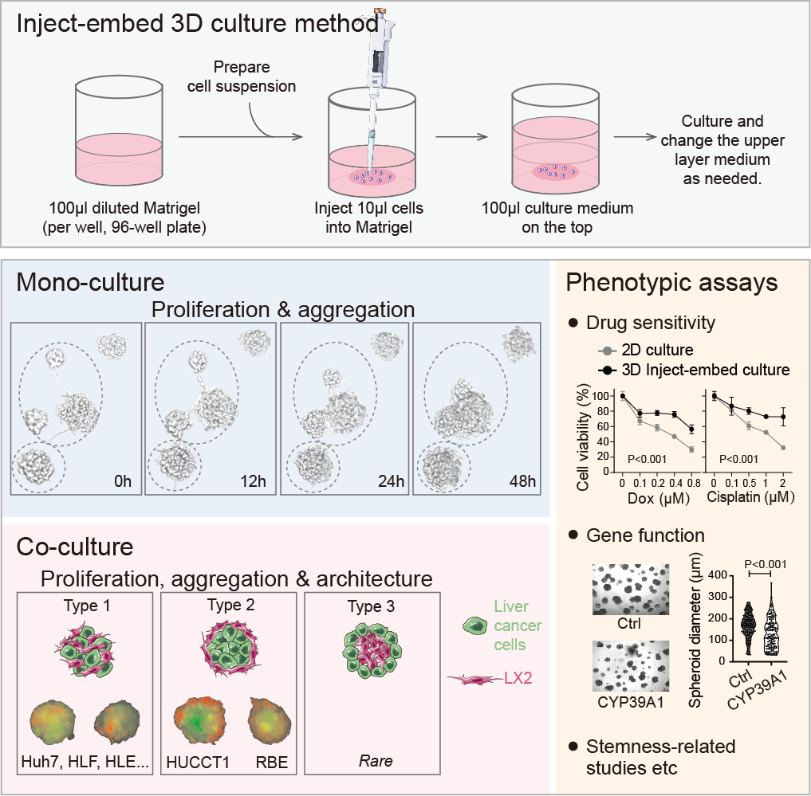
Fig 1. Inject-embed三维培养方法示意图及其表型与应用
体外细胞培养与体内动物实验是肿瘤功能研究的两类核心手段。传统二维(2D)培养中,细胞以单层方式附着于平面生长,难以真实反映肿瘤组织的三维结构与代谢梯度;动物实验虽更接近体内环境,但成本高、周期长,且对关键中间过程的精细操控存在局限。近年来三维(3D)细胞培养快速发展,可在一定程度上模拟肿瘤组织,但对肿瘤微环境的模拟仍面临挑战。
本研究在经典的三维细胞培养策略基础上,建立了新的“inject-embed”三维培养平台:将单一或多种细胞悬浮于培养基中后注入Matrigel混合物,构建兼具“液体界面”与“固体界面”的培养环境,从而同时支持细胞-细胞、细胞-基质互作,并形成标准化的操作流程与可量化评价体系。
研究采用7种细胞系对平台进行验证,包括6株原发性肝癌细胞系(4株肝细胞癌HCC、2株胆管癌CCA)以及代表肝癌微环境中肿瘤相关成纤维细胞重要来源的活化肝星状细胞LX2。单独培养条件下,所有细胞系均可形成3D球体(spheroids),其大小与形态呈细胞系依赖性差异;共培养条件下,肝癌细胞与LX2可形成具有特征性空间组织的3D聚集体(aggregates):HCC与LX2主要形成混合型LX2-HCC杂合聚集体,而CCA与LX2则更倾向形成“CCA居中、LX2环绕”的有序结构。无论单独培养还是共培养,inject-embed体系均支持细胞增殖与3D结构进一步组装,并促进细胞间通讯。
与2D培养相比,细胞在该3D体系中呈现转录表达谱改变,干性相关基因表达增强,并表现出更高的化疗药物耐受性;此外,已知HCC恶性调控因子的干预可改变球体大小与数量,进一步提示该平台适用于肿瘤相关功能研究与表型评估。
总体而言,“inject-embed”方法具有良好的可重复性与可操作性,可促进球体/聚集体的生长与组装并形成特异三维架构,为在更接近肿瘤微环境条件下研究肿瘤恶性、干性及药物反应提供了新的体外模型与技术路径。
浙江大学张涵远博士与薛淑婷博士为共同第一作者。我院姬峻芳教授与虞朝辉教授(浙江大学医学院附属第一医院消化内科)为共同通讯作者。本研究由九游(中国)一站式服务平台与团队合作完成并联合发表。该研究获得国家自然科学项目和浙江省领雁重大项目等基金资助。
原文链接:https://link.springer.com/article/10.1186/s12935-026-04250-1