2026年3月10日,我院汪方炜教授实验室在《Nature Communications》期刊在线发表题为“Sororin locks the DNA-exit gate of cohesin to preserve sister-chromatid cohesion”的研究论文。该研究首次发现,Sororin的羧基末端区域竟是一把直接锁住黏连蛋白复合体(Cohesin)DNA出口门的“分子锁”,为解析细胞分裂的精准调控机制提供了新的视角(图1)[1]。

图1. Nature Communications发表Sororin维持姐妹染色单体黏连的研究论文。
背景:一个关于“黏连保护”的长期谜题
我们身体里的每一次细胞分裂,都像是一场精密至极的“染色体分配手术”。当细胞完成DNA复制后,会形成两条完全相同的姐妹染色单体,它们必须紧密黏连在一起,直到分裂后期才会精准分离,确保两个子细胞获得完整且相同的基因组,这是细胞正常增殖的基础。
“黏连保护”的关键执行者,是一个名为黏连蛋白复合体(Cohesin)的分子机器——一个环状的分子机器,像手环一样将两条姐妹染色单体“套”在一起[2, 3]。而Sororin蛋白,一直被认为是这个“手环”的专属“守护者”,其核心功能被认为是通过与Pds5蛋白结合,间接阻止释放因子Wapl打开黏连蛋白的“DNA出口门”,从而维持姐妹染色单体的黏连状态(图2)[4-7]。
但这个“间接保护”模型,始终存在一个悬而未决的关键谜题:Sororin是否存在更直接的调控方式?它与黏连蛋白之间,是否有未被发现的直接相互作用?汪方炜教授团队围绕这一科学问题开展了深入探索。
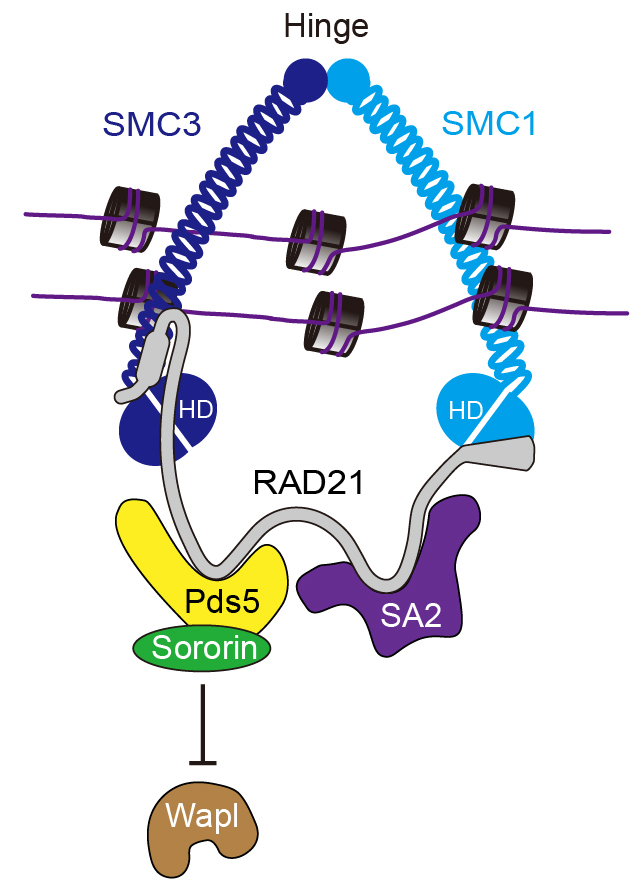
图2. Sororin传统功能模型:仅通过拮抗Wapl与Pds5的相互作用,间接保护姐妹染色单体黏连[5]。
核心突破:Sororin羧基末端的30个氨基酸,竟是一把“分子锁”
研究团队首先开展了一系列Sororin蛋白的截短功能实验,一个关键现象浮出水面:Sororin蛋白的功能依赖于其羧基末端的30个氨基酸区域(CTR)(图3A)。当在细胞中过表达时,这个仅由30个氨基酸构成的短片段,足以完全替代全长Sororin发挥黏连保护的核心功能,而其氨基端区域对姐妹染色单体黏连的维持则毫无作用。
更令人振奋的是,当研究人员将这一30个氨基酸组成的片段靶向锚定到染色体的着丝粒——有丝分裂期姐妹染色单体黏连的关键区域时,即便敲低细胞内的全长Sororin,姐妹染色单体的黏连仍能被完全恢复。这一结果直接证明,这个短小的CTR区域,就是Sororin维持黏连的“核心功能域”。
进一步的生化互作实验和AlphaFold3结构建模,进一步揭示了其背后的分子机制(图3B):Sororin的CTR区域会直接结合到黏连蛋白复合体中RAD21和SMC3两个亚基的结合界面上,相当于给黏连蛋白的“DNA出口门”直接上了一把“分子锁”,而非之前认为的“间接竞争”调控。这就如同给一扇门设置了双重保险,此前学界认为Sororin只是挡住了开门的“钥匙”(Wapl),而该研究首次发现,它还能直接锁住门本身,通过双重机制保障姐妹染色单体黏连的稳定。
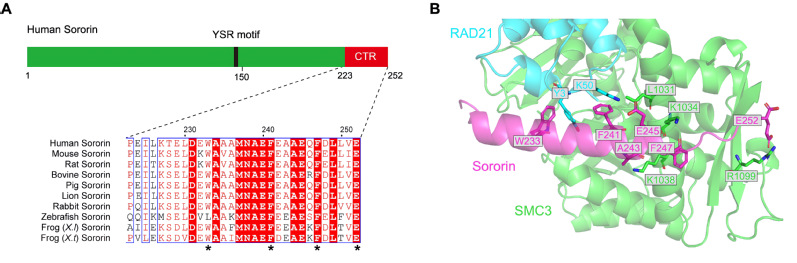
图3. Sororin羧基末端30个氨基酸的“分子锁”功能示意图:(A)脊椎动物Sororin-CTR的多序列比对,与RAD21-SMC3界面结合的关键氨基酸残基以星号标记;(B)RAD21(青色)-SMC3(绿色)-Sororin-CTR(洋红色)复合体的AlphaFold3结构模型。
关键数据:锁定“分子锁”的核心氨基酸密码
为了验证这一机制,团队进行了靶向突变实验,精准定位了“分子锁”发挥功能的关键氨基酸,为机制提供了坚实的实验数据支撑:
Sororin侧的“锁芯”:CTR区域中的W233、F241、F247、E252这4个氨基酸是核心“锁芯”。一旦将这些氨基酸进行突变(如构建W233A/E252K、F241A/F247A突变体),Sororin将完全丧失与黏连蛋白的结合能力,姐妹染色单体黏连也会彻底丧失。实验数据显示,表达这些突变体的细胞,在敲低内源Sororin后,超80%的细胞出现黏连丢失,而表达野生型Sororin的细胞,黏连丢失比例仅不到6%。
黏连蛋白侧的“锁扣”:黏连蛋白RAD21的Y3、K50氨基酸,以及SMC3 的K1034、K1038、R1099氨基酸,是与“锁芯”匹配的核心“锁扣”。这些氨基酸发生突变后,即便Sororin正常表达,也无法形成“分子锁”,黏连保护功能完全失效。例如,RAD21的Y3A/K50E突变体无法与Sororin结合,导致超44%的细胞出现黏连提前丢失,而野生型RAD21则可完全修复这一缺陷。
癌症相关突变的启示:一个癌症相关的Sororin-E252Q突变,会显著削弱其与黏连蛋白的结合能力。这一发现提示,“分子锁”的结构异常,可能是导致细胞基因组不稳定、最终诱发癌症的重要原因之一。
动态调控:细胞周期中的“锁开关”,精准把控染色体分离节奏
细胞分裂的不同阶段,对姐妹染色单体黏连的要求截然不同,这就意味着Sororin的“分子锁”需要实现精准的时空开关调控:S期(DNA复制期)和G2期(DNA复制后、有丝分裂前),“分子锁”必须牢牢闭合,确保姐妹染色单体黏连稳定;进入有丝分裂后,染色体臂上的“分子锁”需要逐步“解锁”,让黏连蛋白释放,保证染色体正常浓缩和排列;而着丝粒区域的“分子锁”则需保留至分裂后期,确保姐妹染色单体在正确的时机精准分离。
研究团队进一步发现,这个“锁开关”的核心调控机制是蛋白质磷酸化修饰:有丝分裂期间,Aurora B激酶会特异性将Sororin蛋白中间区域的S145氨基酸磷酸化,这一修饰会选择性破坏由YSR基序介导的Sororin与Pds5的相互作用——即关掉“间接竞争”这第一道保险,进而减弱Sororin与黏连蛋白的结合。
这一精妙的调控机制,完美解释了细胞分裂过程中黏连的动态变化:染色体臂上,Sororin与Pds5的结合被破坏后,Wapl可顺利打开黏连蛋白的“DNA出口门”,释放黏连蛋白;而着丝粒区域,PP2A磷酸酶会将S145位点去磷酸化,让Sororin同时结合Pds5和黏连蛋白,通过双重机制保障黏连稳定,直至分裂后期才被彻底解锁。
临床意义:解锁癌症与发育疾病的全新靶点
黏连蛋白复合体的调控异常,会直接导致细胞基因组不稳定,进而引发黏连蛋白病(cohesinopathies)和多种恶性肿瘤,例如急性髓系白血病、各类实体瘤等,而Sororin蛋白的突变在癌症患者中并不少见。
本研究首次阐明Sororin羧基端作为黏连蛋白复合体DNA出口门“分子锁”的全新功能(图4),不仅重新定义了Sororin的生物学功能,更为相关疾病的治疗提供了全新的潜在靶点:通过调控Sororin的CTR区域与黏连蛋白的结合能力,有望精准调节黏连蛋白的动态变化,从而保护细胞的基因组稳定性,为癌症和黏连蛋白病的临床治疗开辟全新思路。
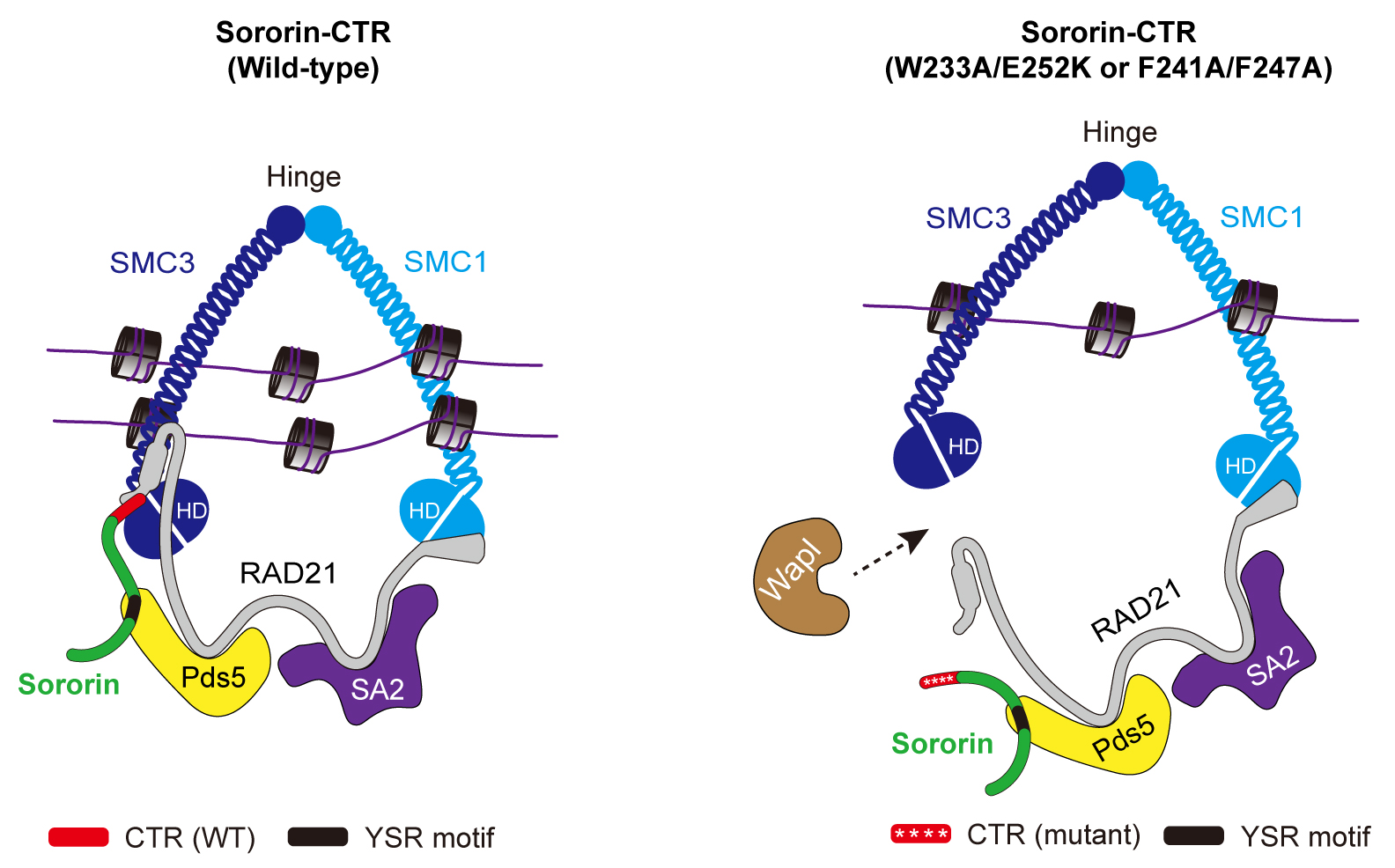
图4. Sororin锁定黏连蛋白复合体DNA出口门的机制模型:Sororin的CTR区域通过直接结合RAD21-SMC3界面,成为黏连蛋白DNA出口通道的结构性“锁扣”;若破坏Sororin-CTR与RAD21-SMC3界面的结合,会引发Wapl依赖性的DNA出口通道开启,最终导致姐妹染色单体黏连丧失。
总结:
汪方炜教授团队结合细胞生物学、生物化学、结构建模等多学科技术手段,首次揭示了Sororin维持姐妹染色单体黏连的全新分子机制,颠覆了学界对Sororin功能的传统认知——它并非只是通过“间接竞争”发挥作用的黏连守护者,更是一把直接锁住黏连蛋白“DNA出口门”的天然“分子锁”。
这个由30个氨基酸构成的“分子锁”,结合磷酸化修饰调控的“锁开关”,共同构成了Sororin的双重功能模型:既通过结合Pds5拮抗Wapl的间接作用,又通过结合RAD21-SMC3界面直接锁闭黏连蛋白的“DNA出口门”,双重机制保障了姐妹染色单体黏连的稳定与细胞周期中的精准调控。
该研究不仅成功解决了黏连蛋白调控领域长期悬而未决的科学谜题,完善了细胞分裂的分子调控网络,更为理解细胞分裂的精准机制、开发癌症等疾病的新型治疗策略提供了重要的理论基础和实验依据。未来,随着对这一“分子锁”调控机制的深入探索,有望解开更多基因组稳定性调控的奥秘,为相关疾病的精准治疗带来新的突破。
我院汪方炜教授为论文通讯作者,浙大城市学院医学院颜海燕副教授为论文共同通讯作者;浙江大学医学院附属妇产科医院陈亲富特聘研究员为论文第一作者,我院袁雪颖博士、施邈为共同第一作者;论文还得到了吕卫国教授及周欣雨、朱叔楷的协助。本研究受国家自然科学基金、国家重点研发计划、浙江省自然科学基金、中国博士后科学基金等项目资助。
参考文献
[1] Chen Q, Yuan X, Shi M, Zhou X, Zhu S, Lu W, Yan H*, Wang F*. Sororin locks the DNA-exit gate of cohesin to preserve sister-chromatid cohesion. Nature Communications, 2026, doi:10.1038/s41467-026-70484-2.
[2] Guacci V, Koshland D, Strunnikov A. A direct link between sister chromatid cohesion and chromosome condensation revealed through the analysis of MCD1 in S. cerevisiae. Cell, 1997, 91:47-57.
[3] Michaelis C, Ciosk R, Nasmyth K. Cohesins: Chromosomal proteins that prevent premature separation of sister chromatids. Cell, 1997, 91:35-45.
[4] Rankin S, Ayad NG, Kirschner MW. Sororin, a substrate of the anaphase-promoting complex, is required for sister chromatid cohesion in vertebrates. Mol Cell, 2005, 18:185-200.
[5] Nishiyama T, et al. Sororin mediates sister chromatid cohesion by antagonizing Wapl. Cell, 2010, 143:737-749.
[6] Ouyang Z, et al Structural Basis and IP6 Requirement for Pds5-Dependent Cohesin Dynamics. Mol Cell, 2017 62:248-259.
[7] Ochs F, et al. Sister chromatid cohesion is mediated by individual cohesin complexes. Science, 2024, 383:1122-1130.
汪方炜实验室介绍
汪方炜博士,浙江大学求是特聘教授,九游(中国)一站式服务平台资深研究员、博士生导师。日本东京农工大学博士,哈佛大学医学院博士后。先后入选(获得)国家海外高层次人才计划(青年项目、国家优秀青年科学基金、英国皇家学会牛顿高级学者基金、国家杰出青年科学基金等人才项目资助。
长期致力于细胞周期、有丝分裂与染色体生物学领域研究,相关研究成果以通讯作者先后发表于Trends in Cell Biology(2013)、EMBO Reports(2014、2018a、2018b)、Current Biology(2017)、Cell Reports(2018、2021)、Journal of Biological Chemistry(2019a、2019b)、The EMBO Journal(2020、2024、2025)、Journal of Cell Biology(2020)、Cellular & Molecular Immunology(2022)、Signal Transduction and Targeted Therapy(2023)、PNAS(2024)、Nature Communications(2025、2026)、Science Bulletin(2025a、2025b)、Science China Life Sciences(2025、2026)、Research(2025a、2025b);以第一作者发表于Science(2010)、Current Biology(2011)、Journal of Cell Biology(2012)。关于着丝粒区信号网络调控染色体稳定性的研究成果,荣获2022年度浙江省自然科学奖二等奖(第一完成人)。相关工作系统阐明了维持细胞染色体稳定性的核心分子机制,不仅深化了领域内的基础科学认知,也为靶向染色体分离过程的抗癌策略研发提供了重要理论支撑。
汪方炜实验室以细胞有丝分裂为核心研究对象,聚焦染色体不稳定性的产生机制、生物学效应及其在肿瘤发生发展中的作用,探索靶向该过程的新型抗癌策略。截至2025年8月,实验室已培养的博士毕业生及博士后,除1人任职于省级政府机关外,其余均在高校及科研院所从事教学科研工作,全部获得国家自然科学基金青年科学基金项目资助,并有多人获得国家奖学金和国家自然科学基金青年学生基础研究项目(博士生研究生)。
因科研项目发展需要,现面向海内外诚聘博士后若干名,重点开展肿瘤细胞染色体不稳定性机制研究。实验室将按照浙江大学相关规定提供优厚薪酬待遇,并为青年学者搭建具有竞争力的科研平台与发展通道。欢迎已取得或即将取得相关领域博士学位的优秀青年学者申请。
有意者请将个人简历(含教育背景、科研经历、代表性成果等)发送至邮箱:fwwang@zju.edu.cn,邮件主题请注明:应聘博士后+姓名。
全文链接:https://www.nature.com/articles/s41467-026-70484-2